Alkany
Alkany (parafiny, z łac. parum affinis = mało powinowaty[1][2]) – łańcuchowe węglowodory nasycone, organiczne związki chemiczne zbudowane wyłącznie z atomów węgla i wodoru, przy czym atomy węgla połączone są ze sobą wyłącznie wiązaniami pojedynczymi[3]. Ogólny wzór sumaryczny alkanów ma postać C
nH
2n+2.
Według obowiązującej systematyki IUPAC węglowe łańcuchy atomów w cząsteczkach alkanów mogą być zarówno proste, jak i rozgałęzione, jednak nie mogą tworzyć pierścieni ani zamkniętych pętli – cykloalkany nie są zatem alkanami[3][4].
Grupa alkanów uszeregowana według długości łańcuchów węglowych stanowi szereg homologiczny alkanów. Dalsze elementy tego szeregu określane są jako wyższe alkany (według różnych kryteriów jako wyższe alkany przyjmuje się np. homologi o łańcuchu >C6, >C10 lub >C16).
Rodzaje łańcuchów alkanów
Alkany zawierające więcej niż trzy atomy węgla mogą tworzyć wiele izomerów konstytucyjnych różniących się rozgałęzieniami łańcuchów węglowych.
Łańcuchy proste
Atomy węgla tworzą jeden nierozgałęziony łańcuch, na którego obydwu końcach znajdują się grupy metylowe.
Ze względu na możliwość rotacji wokół pojedynczych wiązań C−C, związki te mogą tworzyć izomery konformacyjne. Najniższą energię, a co za tym idzie, najwyższą trwałość mają konfromery, w których wiązania znajdują się w układzie naprzemianległym, a atomy węgla znajdują się w pozycjach antiperipalanarnych (trans). W warunkach normalnych zmiany konformacji alkanów następują bardzo szybko i nie można wyizolować poszczególnych konformerów[5].
Przykładowe konformacje naprzemianległe n-pentanu (deskryptory określają kąt torsyjny dla atomów C
1−C
2−C
3−C
4 i C
2−C
3−C
4−C
5:
Łańcuchy rozgałęzione
Co najmniej jeden z atomów węgla jest związany z więcej niż dwoma innymi atomami węgla, cała cząsteczka zawiera więcej niż dwie grupy metylowe.
Przykłady dla pięciu atomów węgla – rozgałęzione izomery konstytucyjne pentanu:
Liczba istniejących izomerów konstytucyjnych węglowodorów o łańcuchach rozgałęzionych rośnie bardzo szybko wraz z liczbą atomów węgla tworzących cząsteczkę. W powyższym przykładzie alkanów zawierających 5 atomów węgla, są to 3 izomery: n-pentan, izopentan i neopentan. Proste obliczenia kombinatoryczne (stabelaryzowane w OEIS) pozwalają wyznaczyć teoretyczną liczbę takich izomerów konstytucyjnych dla dowolnej liczby atomów węgla[6].
| Nazwa | Liczba izomerów |
|---|---|
| Metan | 1 |
| Etan | 1 |
| Propan | 1 |
| Butan | 2 |
| Pentan | 3 |
| Heksan | 5 |
| Heptan | 9 |
| Oktan | 18 |
| Nonan | 35 |
| Dekan | 75 |
| Undekan | 159 |
| Heksadekan | 10 359 |
| Nonatriakontan | 23 647 478 933 969 |
| Hektan | 59×1038 |
W praktyce część izomerów jest jednak niestabilna.
Łańcuchy cykliczne
Zgodnie z systematyką IUPAC, cząsteczki zawierające łańcuchy cykliczne (cykloalkany, nazywane czasem alkanami cyklicznymi) formalnie nie należą do alkanów.
Właściwości
Alkany są słabo rozpuszczalne w wodzie (rozpuszczalność rzędu kilkudziesięciu miligramów na litr), rozpuszczają się w rozpuszczalnikach organicznych. Są mało reaktywne ze względu na dużą trwałość wiązań C−C i C−H. Podobne właściwości do alkanów mają również cykloalkany (z wyjątkiem cyklopropanu i cyklobutanu, które są nietrwałe z powodu silnych naprężeń w małych pierścieniach ich cząsteczek).
Stany skupienia
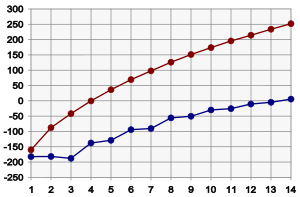
W zależności od temperatury oraz ciśnienia każdy z alkanów może być gazem, cieczą lub ciałem stałym. Temperatury przejść fazowych pomiędzy tymi stanami skupienia dla pierwszych czternastu alkanów o łańcuchach prostych przedstawia rysunek. Jak widać, temperatura wrzenia tych związków rośnie monotonicznie ze wzrostem długości łańcucha (liczby atomów węgla), natomiast temperatura topnienia rośnie monotonicznie począwszy od propanu.
Spośród alkanów i cykloalkanów o tej samej liczbie atomów węgla, temperatura wrzenia cykloalkanu jest wyższa niż odpowiedniego alkanu liniowego[7], natomiast temperatury wrzenia alkanów o łańcuchach rozgałęzionych są niższe niż alkanu liniowego[8]. Tę ostatnią regularność można wytłumaczyć zmniejszeniem powierzchni cząsteczek rozgałęzionych w stosunku do liniowych, przez co obniża się liczba oddziaływań międzycząsteczkowych, a więc ich pokonanie staje się możliwe w niższych temperaturach[8].
W temperaturze pokojowej (25 °C) alkany liniowe lżejsze od pentanu (tj. zawierające 1–4 atomów węgla) są gazami, dalsze homologi – od pentanu do heptadekanu (5–17 atomów C) są cieczami, a oktadekan i cięższe (≥18 atomów C) są ciałami stałymi[7].
Najważniejsze reakcje
Nazwa węglowodory nasycone wynika z faktu pełnego wysycenia atomów węgla wiązaniami pojedynczymi, co odróżnia je od węglowodorów nienasyconych, posiadających wiązania podwójne i/lub potrójne.
Ze względu na dużą trwałość pojedynczych wiązań C−C i C−H alkany są mało reaktywnymi związkami chemicznymi, a reakcje z ich udziałem wymagają drastycznych warunków (wysokich temperatur i ciśnienień). Generalnie wyróżnia się trzy typy reakcji, którym ulegają alkany[9][10]:
- spalanie
- spalanie całkowite – produkty spalania to dwutlenek węgla i para wodna (woda); na przykładzie metanu:
- CH
4 + 2O
2 → CO
2 + 2H
2O
- spalanie niecałkowite – w skład spalin wchodzą także produkty utlenione częściowo, np. tlenek węgla lub sadza (węgiel)
- halogenowanie rodnikowe (substytucja) – powstają pochodne alkanów, na przykład:
- CH
4 + Cl
2 → CH
3Cl + HCl – reakcja metanu z chlorem, w wyniku której powstaje chlorometan i chlorowodór
- piroliza prowadząca do zmniejszenia długości łańcuchów węgla w cząsteczkach oraz do ich izomeryzacji. Reakcje te mają duże znaczenie praktyczne przy produkcji paliw ciekłych (kraking, reforming).
Nazewnictwo alkanów
Nazwa alkanu składa się z trzech części:
- przedrostka i/lub wrostka – lokantu podstawnika
- rdzenia – liczby atomów węgla w łańcuchu głównym
- przyrostka „-an” (przewidzianego dla alkanów).
Etapy nazywania alkanu:
- Wyszukanie macierzystego związku.
- Znalezienie najdłuższego łańcucha atomów węgla (jeżeli dwa różne łańcuchy mają identyczną długość, wybiera się ten z największą liczbą rozgałęzień).
- Numeracja w łańcuchu głównym:
- Atomy węgla numeruje się od końca najbliższego pierwszemu rozgałęzieniu.
- Jeżeli rozgałęzienia występują w równej długości od końców, numeruje się od końca bliższego drugiemu rozgałęzieniu.
- Określenie i numeracja podstawników:
- Każdy podstawnik oznacza się zgodnie z miejscem przyłączenia do łańcucha głównego.
- Jeżeli do danego atomu węgla są przyłączone dwa podstawniki lub więcej, przypisuje się im tę samą cyfrę.
- Zapis nazwy związku
- Podstawniki podaje się w kolejności alfabetycznej, przy czym:
- przedrostek „izo-” (np. izobutyl) włączany jest do nazwy i pierwszą literą jest „i”
- pozostałe przedrostki (np. sec, tert; np. tert-butyl) i ich skróty (s, t; np. tBu) oraz lokanty liczbowe nie są włączane do nazwy, a więc np. dla tert-butyl pierwszą literą jest „b”.
- Całą nazwę zapisuje się w postaci jednego słowa, przy czym:
- do oddzielenia przedrostów i/lub wrostków używa się łącznika (-)
- do rozdzielenia lokantów używa się przecinka (,)
- Podstawniki podaje się w kolejności alfabetycznej, przy czym:
Przykład: 2,2-dimetylobutan
- „2,2” – lokanty podstawników (oba podstawniki są przy tym samym atomie węgla, dlatego oznaczone są tą samą liczbą)
- „di” – liczba podstawników danego rodzaju przy danym atomie węgla („di-”, „tri-”, „tetra-”)
- „metylo” – nazwa podstawników (tutaj są to grupy metylowe)
- „butan” – nazwa alkanu, który ma tyle samo atomów węgla, ile łańcuch główny.
| lp. | Nazwa alkanu | lp. | Nazwa alkanu | lp. | Nazwa alkanu | lp. | Nazwa alkanu |
|---|---|---|---|---|---|---|---|
| 1 | metan | 26 | heksakozan | 51 | henpentakontan | 76 | heksaheptakontan |
| 2 | etan | 27 | heptakozan | 52 | dopentakontan | 77 | heptaheptakontan |
| 3 | propan | 28 | oktakozan | 53 | tripentakontan | 78 | oktaheptakontan |
| 4 | butan | 29 | nonakozan | 54 | tetrapentakontan | 79 | nonaheptakontan |
| 5 | pentan | 30 | triakontan | 55 | pentapentakontan | 80 | oktakontan |
| 6 | heksan | 31 | hentriakontan | 56 | heksapentakontan | 81 | henoktakontan |
| 7 | heptan | 32 | dotriakontan | 57 | heptapentakontan | 82 | dooktakontan |
| 8 | oktan | 33 | tritriakontan | 58 | oktapentakontan | 83 | trioktakontan |
| 9 | nonan | 34 | tetratriakontan | 59 | nonapentakontan | 84 | tetraoktakontan |
| 10 | dekan | 35 | pentatriakontan | 60 | heksakontan | 85 | pentaoktakontan |
| 11 | undekan | 36 | heksatriakontan | 61 | henheksakontan | 86 | heksaoktakontan |
| 12 | dodekan | 37 | heptatriakontan | 62 | doheksakontan | 87 | heptaoktakontan |
| 13 | tridekan | 38 | oktatriakontan | 63 | triheksakontan | 88 | oktaoktakontan |
| 14 | tetradekan | 39 | nonatriakontan | 64 | tetraheksakontan | 89 | nonaoktakontan |
| 15 | pentadekan | 40 | tetrakontan | 65 | pentaheksakontan | 90 | nonakontan |
| 16 | heksadekan | 41 | hentetrakontan | 66 | heksaheksakontan | 91 | hennonakontan |
| 17 | heptadekan | 42 | dotetrakontan | 67 | heptaheksakontan | 92 | dononakontan |
| 18 | oktadekan | 43 | tritetrakontan | 68 | oktaheksakontan | 93 | trinonakontan |
| 19 | nonadekan | 44 | tetratetrakontan | 69 | nonaheksakontan | 94 | tetranonakontan |
| 20 | eikozan | 45 | pentatetrakontan | 70 | heptakontan | 95 | pentanonakontan |
| 21 | heneikozan | 46 | heksatetrakontan | 71 | henheptakontan | 96 | heksanonakontan |
| 22 | dokozan | 47 | heptatetrakontan | 72 | doheptakontan | 97 | heptanonakontan |
| 23 | trikozan | 48 | oktatetrakontan | 73 | triheptakontan | 98 | oktanonakontan |
| 24 | tetrakozan | 49 | nonatetrakontan | 74 | tetraheptakontan | 99 | nonanonakontan |
| 25 | pentakozan | 50 | pentakontan | 75 | pentaheptakontan | 100 | hektan |
Zobacz też
- wyższe alkany
- alkeny
- alkiny
- alkanosulfoniany
- reakcja Wurtza
Przypisy
- ↑ parafina. Słownik wyrazów obcych PWN. [dostęp 2016-02-13]. [zarchiwizowane z tego adresu (2014-02-22)].
- ↑ Witold Doroszewski (red.): parafina. [w:] Słownik języka polskiego [on-line]. PWN. [dostęp 2016-02-13].
- ↑ a b alkanes, [w:] A.D. McNaught, A. Wilkinson, Compendium of Chemical Terminology (Gold Book), S.J. Chalk (akt.), International Union of Pure and Applied Chemistry, wyd. 2, Oxford: Blackwell Scientific Publications, 1997, DOI: 10.1351/goldbook.A00222, ISBN 0-9678550-9-8 (ang.).
- ↑ cycloalkanes, [w:] A.D. McNaught, A. Wilkinson, Compendium of Chemical Terminology (Gold Book), S.J. Chalk (akt.), International Union of Pure and Applied Chemistry, wyd. 2, Oxford: Blackwell Scientific Publications, 1997, DOI: 10.1351/goldbook.C01497, ISBN 0-9678550-9-8 (ang.).
- ↑ Robert T. Morrison, Robert N. Boyd: Chemia organiczna. T. 1. Warszawa: PWN, 1985, s. 105–110, 179–181. ISBN 83-01-04166-8.
- ↑ Number of n-node unrooted quartic trees; number of n-carbon alkanes C(n)H(2n+2) ignoring stereoisomers. The On-Line Encyclopedia of Integer Sequences. [dostęp 2010-10-04]. (ang.).
- ↑ a b Robert T. Morrison, Robert N. Boyd: Chemia organiczna. T. 1. Warszawa: PWN, 1985, s. 117 i 342. ISBN 83-01-04166-8.
- ↑ a b Robert T. Morrison, Robert N. Boyd: Chemia organiczna. T. 1. Warszawa: PWN, 1985, s. 118. ISBN 83-01-04166-8.
- ↑ Robert T. Morrison, Robert N. Boyd: Chemia organiczna. T. 1. Warszawa: PWN, 1985, s. 128–146. ISBN 83-01-04166-8.
- ↑ Produkty spalania. warter.pl. [zarchiwizowane z tego adresu (2016-06-25)].. Zakłady Chemiczne Warter. Dostęp: 2016-11-06.
Media użyte na tej stronie
n-pentan trans-trans.
Melting points (in blue) and boiling points (in pink) of the first fourteen alkanes (temperatures in °C, number of carbon atoms along the horizontal axis)
Gauche(+)-gauche(+) conformation of normal pentane
Autor: Autor nie został podany w rozpoznawalny automatycznie sposób. Założono, że to MesserWoland (w oparciu o szablon praw autorskich)., Licencja: CC-BY-SA-3.0
Trans-gauche conformation of normal pentane











